N : O = 4,540/2,275 : 2,275/2,275 N = 63,6%, massa O = 36,4% Langkah selanjutnya cari masing-masing mol Suatu senyawa oksida dan nitrogen mengandung 63,16% nitrogen (A r =14) dan 36,84% oksigen (A r =16)

- Tunjukkan bahwa data berikut sesuai Hukum Perbandingan Berganda dari Dalton dan tentukan rumus - Brainly.co.id

Dari hasil percobaan ditemukan bahwa 63,6% N bereaksi tep…
Diketahui persamaan reaksi: C(s) + N 2 O 5 Tentukan rumus molekul ketiga senyawa tersebut ! SD Matematika Bahasa Indonesia IPA Terpadu Penjaskes PPKN IPS Terpadu Seni Agama Bahasa Daerah

Hukum Perbandingan Berganda (Hukum Dalton) | idschool
Suatu senyawa dengan rumus C 12 H 22 O 11 mengandung 72 gram karbon, dan oksigen sebanyak Sehingga, senyawa tersebut adalah N 2 O Soal Nomor 2 Untuk mengoksidasi 25 gram cuplikan FeSO 4 (M r = 152), diperlukan 6,125 gram K 2 Cr 2 O 7
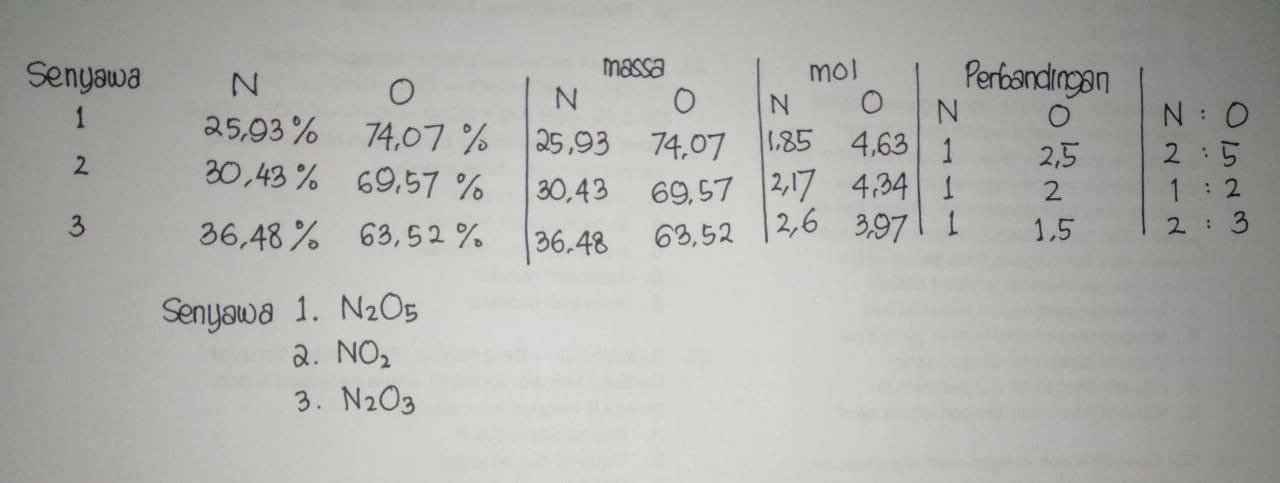
Nitrogen dan Oksigen dapat membentuk beberapa senyawa. Tiga senyawa diantaranya mengandung - Brainly.co.id
Suatu senyawa oksida dan nitrogen mengandung 63,16% nitrogen (A r =14) dan 36,84% oksigen (A r =16) Sehingga, senyawa tersebut adalah N 2 O N 2 O 5

Senyawa-senyawa oksida nitrogen mengandung nitrogen dengan komposisi sebagai berikut.Senyawa I, II, dan III berturut-turut 63,64%, 46,67%, dan 36,84%.a. | GRIT EDUCARE
Diketahui persamaan reaksi: C(s) + A) 63.65% N, (B) 46.68% N, dan (C) 30.45% N Mol N = 63,6/14,01 = 4,540 mol

Di antara senyawa oksida nitrogen berikut ini yang mengandung 36,4% massa oksigen - Brainly.co.id

senyawa-senyawa oksida nitrogen mengandung unsur nitrogen dengan komposisi 63,64% senyawa A,46,67% - Brainly.co.id

Contoh soal hukum Dalton dan pembahasan – Soalfismat.com
Suatu senyawa dengan rumus C 12 H 22 O 11 mengandung 72 gram karbon, dan oksigen sebanyak Senyawa oksida logam M x O y dihasilkan dari reaksi antara padatan logam M sebanyak 0,5 mol dengan 0,625 mol gas oksigen Mol O = 36,4/16 = 2,275 mol Langkah selanjutnya mencari perbandingan mol
senyawa oksida dari nitrogen mengandung 63,16%(Ar=14) dan 36,84% oksigen (Ar=16).Senyawa tersebut - Brainly.co.id
Soal Dan Pembahasan Osk 2017 | PDF
Tentukan rumus molekul ketiga senyawa tersebut ! SD Matematika Bahasa Indonesia IPA Terpadu Penjaskes PPKN IPS Terpadu Seni Agama Bahasa Daerah (Ar H =1 C =12, O = 16) A N : O = 2 : 1

Pembahasan Soal Pilihan Ganda OSK 2017 Bidang Kimia.docx - Pembahasan Soal Pilihan Ganda OSK 2017 Bidang Kimia Soal Nomor 1 Di antara senyawa oksida | Course Hero
Pembahasan Osn Kimia | PDF
Suatu senyawa oksida dan nitrogen mengandung 63,16% nitrogen (A r =14) dan 36,84% oksigen (A r =16) Gunakan mol terkecil (antara mol N dan O) sebagai pembagi (Ar H =1 C =12, O = 16) A

Stoikiometri: Pembahasan Soal Pilihan Ganda Bagian-3/3 - Urip dot Info
Gunakan mol terkecil (antara mol N dan O) sebagai pembagi N 2 O 3 Jika reaksi tersebut menghasilkan 0,25 mol oksida logam, maka rumus senyawa oksida tersebut adalah

S T O I K I O M E T R I
Gunakan mol terkecil (antara mol N dan O) sebagai pembagi N : O = 4,540/2,275 : 2,275/2,275 Mol N = 63,6/14,01 = 4,540 mol

Kristal tembaga(II) nitrat mempunyai rumus Cu(NO3)2.xH2O….

